Oubliez la perfection chimique. Aucun laboratoire, aussi impeccable soit-il, ne garantit un rendement de purification irréprochable à chaque essai. Pourtant, comprendre comment calculer ce rendement,et éviter les erreurs classiques,reste la clé pour avancer avec confiance dans les protocoles de synthèse organique.
Cours Physique-Chimie | Première spécialité
Ce contenu se rattache directement à la partie « Synthèses des espèces chimiques organiques » du programme de spécialité en première.
Il s’intègre dans le chapitre « Constitution et transformations de la matière, propriétés physico-chimiques, synthèses et transformations d’espèces chimiques organiques ».
Protocole de synthèse organique : étapes et outils
Pour cerner la logique de la synthèse organique, voici les principales séquences à maîtriser :
- Définition d’une synthèse organique
- Rôle et structure d’un protocole
- Étapes majeures de la production en laboratoire
- Gestion des réactifs
- Phase de chauffage sous reflux
- Procédures d’isolement et de purification du produit après synthèse
- Mode de caractérisation du produit obtenu
Rendement de synthèse : repères à retenir
À propos du rendement, il convient de saisir les points suivants :
- Définition du rendement de synthèse
- Méthodes d’évaluation et unités à employer
- Calcul du rendement à partir des données expérimentales
- Interprétation et valeur du rendement
- Calculs à partir des masses et des volumes
- Analyse des causes d’un rendement faible
Pour approfondir, d’autres ressources sur les bases de la spécialité sont disponibles sur cette page.
Journal d’une synthèse organique
Définition de la synthèse organique
Le principe a déjà été évoqué au lycée, lors des premiers cours sur les transformations chimiques.
Pour mémoire, une synthèse consiste à enchaîner différentes opérations impliquant au moins une transformation chimique, dans le but d’obtenir une espèce chimique donnée.
On parle de synthèse organique dès lors que l’espèce à produire appartient à la chimie organique.
Qu’est-ce qu’un protocole ?
Le protocole rassemble l’ensemble des opérations nécessaires à la réalisation d’une synthèse.
Il précise notamment :
- Les réactifs à utiliser, avec leurs quantités respectives
- La verrerie à prévoir (béchers, pipettes…), en détaillant les volumes requis
- Le matériel complémentaire (accessoires, appareils…)
- Les conditions physiques de la transformation (température, pression…)
- La durée estimée pour chaque étape (chauffage, séchage…)
Étapes incontournables d’une synthèse organique
La conduite d’une synthèse organique s’articule autour des moments suivants :
- Préparation des réactifs : pesée ou mesure de volume précise de chaque substance impliquée
- Transformation des réactifs : mise en condition favorable à la réaction chimique
- Isolement et purification du produit : extraction du milieu réactionnel puis élimination des impuretés
- Analyse et caractérisation : vérification, par tests physiques ou chimiques, de la nature du produit obtenu
Préparer les réactifs
Chaque réactif doit être prélevé selon la quantité stipulée dans le protocole.
- Réactif solide : la pesée s’effectue à l’aide d’une balance adaptée, d’une spatule et d’un récipient propre.
- Réactif liquide : la mesure du volume se fait à l’aide d’une pipette graduée ou volumétrique et d’une propipette pour garantir la précision.
Le solvant, quant à lui, demande généralement une mesure moins rigoureuse : une éprouvette graduée suffit souvent.
Si le protocole ne précise pas les quantités de réactifs à employer ?
Dans ce cas, il faut les déterminer :
- En fonction de la quantité de produit à synthétiser
- À partir du tableau d’avancement pour évaluer la progression maximale et la quantité initiale requise
- En prévoyant éventuellement un excès d’un réactif pour faciliter l’isolement ou la purification
Comment obtenir la masse d’un réactif à partir de sa quantité de matière ?
Si la quantité de matière (en moles) est donnée mais pas la masse, on applique la relation :
m = n × M
où :
- n : quantité de matière (mol)
- M : masse molaire du réactif (g·mol⁻¹)
- m : masse à prélever (g)
Calculer le volume d’un réactif liquide à partir de sa quantité de matière
Si la quantité de matière est donnée, la démarche consiste à :
- Calculer d’abord la masse avec m = n × M
- Puis déterminer le volume en utilisant m = ρ × V, où ρ est la densité (g·L⁻¹) et V le volume (L)
Réaliser la réaction
Pour optimiser la réaction chimique, il convient de :
- Utiliser un récipient adapté, souvent un ballon
- Mettre en place les conditions physiques requises (chauffage, agitation…)
- Assurer un bon contact entre les réactifs
- Limiter les pertes pendant le chauffage grâce à un montage approprié (refroidissement à air ou à eau)
Chauffage sous reflux
- Pourquoi chauffer le milieu réactionnel ?
Certaines réactions, comme les précipitations ou combustions, sont rapides. Mais la plupart des transformations organiques nécessitent du temps : la consommation des réactifs peut prendre des minutes, parfois des heures.
Pour accélérer les choses, on chauffe le mélange : la température booste la vitesse de réaction.
Chauffer le milieu réactionnel permet donc de gagner en efficacité.
- Risques d’un simple chauffage
En chauffant, des substances peuvent s’évaporer : réactifs, produits ou solvant s’échappent sous forme de vapeurs.
Conséquence : pertes de matière, rendement en baisse et parfois, risques sanitaires liés aux émanations.
- Principe du chauffage à reflux
Fermer hermétiquement le récipient n’est pas la solution : la pression monterait et le danger d’explosion serait bien réel.
Le chauffage à reflux maintient la pression atmosphérique : les vapeurs montent dans un réfrigérant, se condensent, puis retombent dans le ballon. Rien ne s’échappe, tout reste en circuit.
Le chauffage à reflux s’appuie sur un réfrigérant qui condense les vapeurs et les renvoie dans le milieu réactionnel. Le système fonctionne ainsi en boucle.
On utilise le plus souvent un réfrigérant à eau, parfois un dispositif à air pour des réactions moins exigeantes.
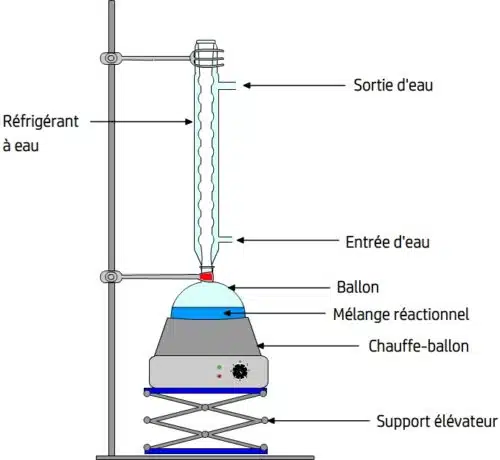
- Chauffage à reflux avec réfrigérant à eau
Le montage comprend :
La tige : stabilise le ballon et le réfrigérant.
Le ballon : accueille les réactifs, assure une chauffe homogène.
Le chauffe-ballon : moteur du chauffage, adapté au ballon.
Le support élévateur : permet de manœuvrer rapidement le ballon, pratique en cas d’incident.
Le réfrigérant à eau : fixé par des pinces, il comporte un canal central (pour la circulation des vapeurs) et des parois creuses où circule de l’eau froide (entrée en bas, sortie en haut vers l’évier).
Chauffage à reflux avec réfrigérant à eau
- Chauffage à reflux avec refroidissement par air
Le dispositif est alors plus simple : moins de matériel requis.
Utile pour les réactions à température modérée ou avec des produits peu volatils.
Ici, l’air ambiant joue le rôle de refroidisseur : le récipient (souvent un Erlenmeyer) est fermé par un bouchon traversé d’un tube de verre (pouvant être une simple pipette).
Les vapeurs se condensent sur le verre refroidi par l’air et retombent dans le mélange.
Isolement et purification du produit de synthèse
Après la synthèse, le produit n’est jamais seul. Il cohabite avec des réactifs non consommés, du solvant, parfois d’autres sous-produits.
D’où la nécessité de l’isoler et de le purifier. La procédure dépend de la nature et des propriétés de chaque substance présente.
Voici les techniques principales utilisées selon les situations rencontrées :
- Filtration : adaptée à l’isolement d’un produit solide séparé du liquide réactionnel sous forme de particules.
- Extraction liquide-liquide (ou extraction par solvant) : permet de récupérer un produit dissous dans le milieu réactionnel.
- Décantation : utilisée pour séparer une espèce organique non miscible avec l’autre phase présente.
- Distillation : efficace pour isoler une espèce chimique liquide lorsque ses propriétés d’ébullition diffèrent clairement de celles du reste du mélange (écart d’au moins 10°C recommandé).
Analyse et caractérisation du produit
Une fois le produit isolé et purifié, il s’agit de vérifier qu’il correspond bien à l’espèce recherchée.
On utilise pour cela différentes méthodes d’analyse chimique ou physique, par exemple :
- Chromatographie : comparaison visuelle d’un échantillon du produit obtenu avec un échantillon de référence, souvent révélée sous lampe UV.
- Mesure de la température de fusion : identification d’un solide par sa température de fusion, déterminée sur une plaque chauffante (type banc Kofler).
Le rendement d’une synthèse
Comment définir le rendement d’une synthèse ?
Le rendement traduit l’efficacité de la synthèse organique. Il mesure la part de produit réellement obtenue par rapport à la quantité maximale théorique possible.
Évaluation et unité
Le rendement est souvent noté η (lettre grecque « eta »), parfois r ou ρ selon les conventions.
Il s’agit d’un rapport sans unité, car il compare deux quantités de même nature.
Calculer le rendement d’une synthèse
Le rendement se définit par le rapport entre la quantité de produit réellement obtenue (Nexp) et la quantité théorique maximale (nmax ou nthéo), calculée en supposant que tout le réactif limitant a réagi selon la stœchiométrie de l’équation.
Où :
- Nexp : quantité de matière du produit réellement obtenue (après isolement et purification), déterminée par mesure de masse ou de volume, exprimée en moles (mol)
- nmax : quantité théorique maximale calculée à partir du tableau d’avancement, en supposant la conversion totale du réactif limitant, également en moles
Pour exprimer le rendement en pourcentage, il suffit de multiplier le résultat précédent par 100.
La formule devient alors :
Valeur du rendement
Par définition, le rendement varie entre 0 (0 %) et 1 (100 %).
Un rendement égal à zéro signifie que rien n’a été obtenu, la synthèse a échoué.
Dans ce cas, plusieurs causes sont à envisager :
- Conditions de réaction non respectées
- Oubli d’un réactif
- Confusion de produits lors de la préparation (par exemple, inversion de béchers)
- Procédures d’isolement ou de purification mal adaptées, ayant éliminé le produit désiré
Un rendement de 1 indique que tout le réactif limitant s’est transformé en produit. Cet idéal reste théorique : dans les faits, chaque étape du protocole entraîne des pertes inévitables et le rendement obtenu est toujours inférieur à 1.
Un rendement supérieur à 1 signale une erreur : problème de calcul, de mesure ou produit mal isolé (présence de solvants, d’autres réactifs ou impuretés non détectées).
Calculer le rendement à partir des masses
La masse d’une espèce chimique est proportionnelle à la quantité de matière :
m = n × M
Le rendement peut donc s’exprimer comme le rapport entre la masse de produit réellement obtenue (mexp) et la masse maximale théorique (mmax) :
Le calcul reste valide à condition d’utiliser la même unité de masse (grammes, milligrammes…)
Calculer le rendement à partir des volumes
Pour une espèce chimique liquide, la masse peut être exprimée en fonction de la densité ρ et du volume V :
m = ρ × V
Le rendement se calcule alors selon la même logique :
En d’autres termes, le rendement peut aussi s’écrire :
Dans le cas d’un produit liquide, le rendement se rapporte alors au volume expérimental (Vexp) sur le volume maximal théorique (Vmax) :
Il faut simplement veiller à utiliser la même unité de volume (litres, millilitres…)
Pourquoi un rendement de synthèse peut-il être faible ?
Différents facteurs peuvent expliquer qu’un rendement soit inférieur à l’espéré :
- Réactifs détériorés lors du stockage, conduisant à une quantité réelle inférieure à celle prévue (par exemple, substances oxydées par l’air)
- Présence d’impuretés dans l’eau distillée ou dans les réactifs eux-mêmes
- Pertes lors des manipulations (transfert de liquides, gouttes résiduelles dans la verrerie…)
- Pertes au moment du chauffage : même sous reflux, certaines espèces volatiles peuvent s’évaporer
- Réaction arrêtée trop tôt : le mélange n’a pas atteint l’avancement maximal, tous les réactifs n’ont pas réagi
- Réaction limitée par un équilibre chimique, empêchant la consommation totale des réactifs (cas des estérifications, par exemple)
- Pertes lors de l’extraction ou de la purification, dues à une technique inadéquate (filtre défectueux, mauvais solvant d’extraction, distillation mal conduite…)
Pour réviser
Pour renforcer vos bases, il est utile de revoir les sujets suivants :
- Corps purs et mélanges
- Catégories d’espèces chimiques
- Mélanges homogènes et hétérogènes
- Tests d’identification chimique
- Chromatographie
- Température d’ébullition et de fusion
- Solutions aqueuses et densité
- Préparation et utilisation des solutions
- Transformation chimique, réactifs et produits
- Écriture et équilibrage des équations de réaction
- Stœchiométrie
Autres chapitres de spécialité à découvrir
- Quantité de matière, masse molaire et concentration
- Réactions d’oxydoréduction et avancement
- Titrage redox
- Diagrammes de Lewis, géométrie moléculaire, électronégativité
- Polarité, cohésion, dissolution, solubilité, affinités hydrophiles ou lipophiles
- Structure et nomenclature des espèces organiques
Pour aller plus loin
- Dossier « Synthèse organique, chimie au service de l’homme », Site Médiachimie
- Phases d’une synthèse organique, Vidéo sur ScholaWebTV (CRDP de Versailles)
Une réaction de synthèse, c’est bien plus qu’un calcul ou une formule : c’est tout un parcours, fait d’essais, d’erreurs, d’ajustements, où chaque étape laisse sa marque sur le rendement obtenu. À chaque expérience, le chimiste affine ses gestes, apprend à repérer la faille, mesure avec justesse l’écart entre théorie et réalité. C’est dans cette différence que se joue l’art de la chimie,et l’exigence, jour après jour, d’atteindre un résultat fidèle, reproductible, maîtrisé.